腸内細菌業のチカラ〜不安や抑うつへの影響とメカニズム

こんにちわ、やま茶です。今日は腸内細菌の役割について解説します。
100〜1000兆個も腸内細菌はヒトの腸内に常在しています。
この莫大な数は、ヒトを構成する細胞37兆個をはるかに上回る数字です。
これらの腸内細菌はヒトの腸内で細菌業(集団)を形成しています。
これらは私たちが思っている以上にとても重要な役割を担っています。
今回はその重要な役割とメカニズムを科学的な視点で解説します。
腸内細菌について〜導入
腸内細菌業は一定のバランスで腸内に常在しています。
このバランスは個人差もありますし、食事やストレス、年齢に寄って変化します。
一般的には、腸内細菌業の70〜75%はフィルミクテス菌群とバクテロイデス菌群が占めています。
他にも1000種程度の菌群が一定のバランスを保って常在しています。
100兆個もある菌の1つ1つが仲間を作って縄張り争いのように菌業を作っているイメージです。
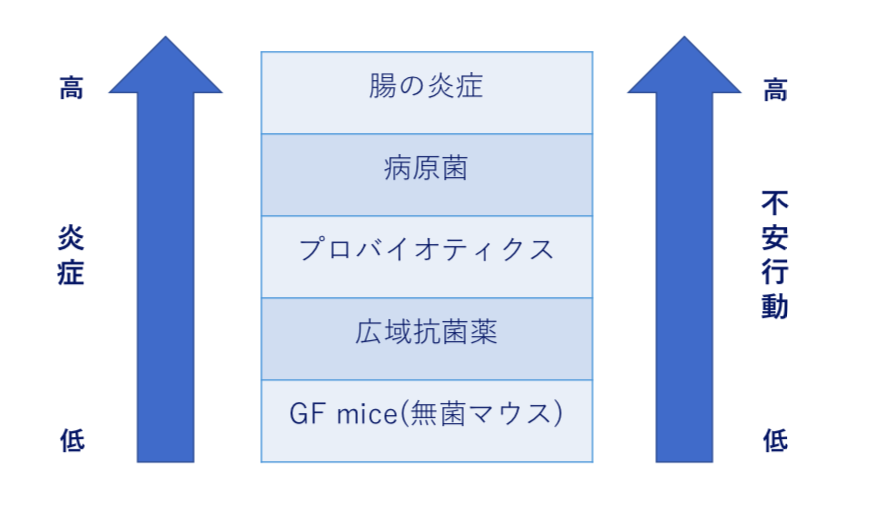
では、腸内細菌がどのような役割を担っているのか明らかにするために、腸内を無菌にしたマウス(以下、GF mice, germ free mice)と病原菌以外の細菌のみ常在しているマウス(以下、SPF mice, specific pathogen free mice)を用いて様々な研究がこれまで行われてきました。
これらのマウスでわかっていることを図で簡略化すると以下のようになります。
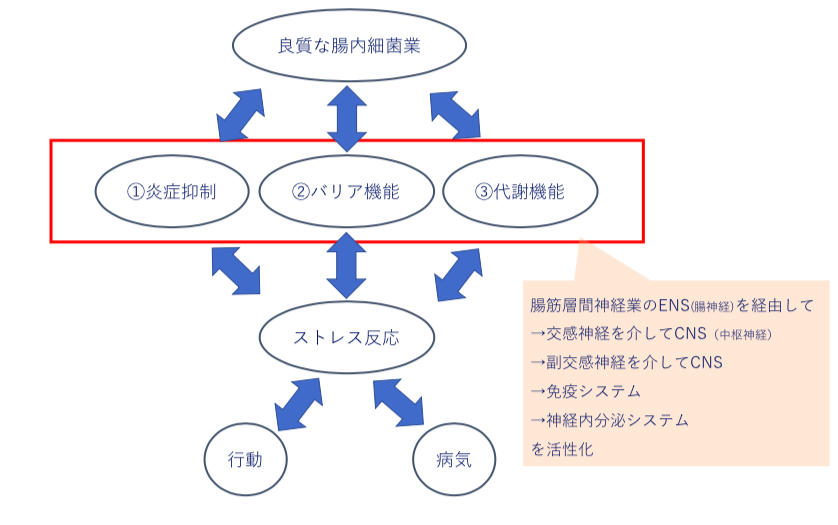
腸内細菌の役割〜①炎症抑制
乳酸菌の摂取(以下、プロバイオティクス)は、腸管透過性を低下させる機能があると言われています。
ストレスなどで腸管透過性が亢進すると細菌が容易に侵入でき、免疫細胞や神経細胞へ接触すると炎症が起きたり、神経内分泌システムが活性化してしまいます。
つまり、乳酸菌によるプロバイオティクスは腸管透過性を低下させることで炎症を抑制したり、うつと関係があると言われている神経内分泌システムであるHPA軸の活性を抑制する作用があります。
炎症と不安の関連は数多くの動物実験で実証されています。
病原菌が侵入すると免疫システムを介さずに不安行動を誘発します。
このメカニズムには炎症が関与していると考えられます。
腸管透過性低下 → 炎症抑制 → 抗不安 ということが示唆されています。
また、広域抗菌薬投与で不安行動が減少したことも観察されています。
これは、腸内細菌業のバランスの変化は常に腸筋層間神経業で感知され、腸神経を介して脳へフィードバックされていることと関与していると言えます。
基本的に脳の神経活動はストレス(良くも悪くも)を生じるため、広域抗菌薬投与で腸内細菌を減らすと脳にフィードバックされるストレス(信号)も減るということなのでしょう。
広域抗菌薬投与後数週間で不安行動も元に戻ることが観察されているので、以上のように考察されます。
何れにせよ、菌は耐性化を獲得するものなので、抗菌薬投与で不安が減るというのは一時的なものであり、長期でみると菌交代現象など感染症のリスク(炎症リスク)もあり、不安行動抑制を目的に使用するのは現実的ではないでしょう。
ここで大事なのは、腸内細菌業のバランスの変化は脳へフィードバックされていることと、プロバイオティクスは腸管透過性を低下させ炎症を抑制し抗不安作用を有する、そして、HPA軸の活性化を抑制し抗うつ効果も有するということです。
幼少期に母子分離を経験した大人のラットにビフィズス菌を投与すると、抗うつ剤(シタロプラム)と同様の抗うつ効果が観察された研究も報告されています。
腸内細菌の役割〜②バリア機能
病原性のあるカンピロバクターを暴露させると不安行動が増えることが報告されています。
これは免疫システムを介したものではなく、感染による炎症が原因だと考えられています。
前述しました通り、腸内細菌群はそれぞれ縄張り争いのようにバランスをとっているので、病原体が少し腸に入ったぐらいでは7割程度占めるとされているフィルミクテス菌群やバクテロイデス菌群に負けてしまいます。
しかし、ストレスなどで腸内細菌業は乱れてしまうので、ストレス下では腸内細菌業のバランスが崩れ縄張りが守れず、腸管透過性も高まり、わずかな病原体の侵入でも感染してしまうこともあります。
腸内細菌業のバランスと中枢神経システムは相互に関連しているということです。
また、感染により腸内細菌業のバランスが変化することで海馬のBDNFが減少することも観察されています。
BDNFは神経のメンテナンスを担う化学物質で、認知機能を維持するための基盤を支えています。
BDNFの低下により認知機能が歪み、不安行動へ影響しているのかもしれません。
BDNFに関しては有酸素運動で増えることもわかっていて過去の記事に書いていますので興味あればこちらも読んでみて下さい。
腸内細菌の役割〜③ 代謝機能
腸内細菌は、多糖を分解しグルコースへ変換しています。
抗菌薬投与で、脂肪炎症マーカーが低下し耐糖能が上がったことから、血糖値と腸内細菌業は関連があると言えます。
血糖値の乱高下はイライラといった症状を誘発するため、腸内細菌業のバランスを良質に維持することが大事だといえます。
乳酸菌やビフィズス菌は、グルタミン酸を代謝しGABAを産生することがわかっています。
GABAといえば、抗不安作用を有する化学物質のことですが、乳酸菌を与えたマウスの中枢神経のストレス関連領域でGABAの受容体発現が変化し、副交感神経を遮断したマウスでは観察されなかったことから副交感神経を介した経路でこれらに影響しているのではないかと考えられています。
また、詳細はわかっていないですが、GF miceの線条体や海馬でセロトニン合成が増えた報告もあるため、腸内細菌業とセロトニンシグナルも関連があるのかもしれません。
ここまでマウスでの研究結果を解説してきました。
ヒトでの腸内細菌業の影響は実際はどうなのでしょうか?
ヒトでの研究は少ないですが、プロバイオティクスの効果を示唆している研究がいくつかあるので紹介します。
プロバイオティクスの有用性
健康成人を対象に、乳酸菌とビフィズス菌を混合したプロバイオティクス群とプラセボ群を二重盲検でランダムに割付し、30日間の投与の後、メンタルヘルスを評価した試験があります2)。
不安や抑うつ、ストレス、対処行動などを質問票で評価したところ、プロバイオティクスを行った群で有意に心理的苦痛が少なかったという結果が出ました。
また、しばしば不安や胃腸障害を合併することがわかっている慢性疲労症候群に注目した研究結果も出ています。
慢性疲労症候群に罹患している方を対象に行われたパイロットスタディでは、2ヶ月間の乳酸菌投与の後、プラセボ群と比較してプロバイオティクス群では有意に不安症状が減ったという報告もあります3)。
腸内細菌と免疫についてはテレビなどでも取り上げられることがありますが、腸内細菌と精神症状についてはどうでしょうか?
この記事を最後まで読んでくださった方には、腸内細菌と精神症状がどのように関連があるのか、お分かりになられたと思います。
メンタルヘルスケアに腸活を取り入れましょう。
以下、参考文献
1) Foster JA, MacVey NeuFeld KA. Trends Neurosci. 2013 May;36(5):305-12.
2) Messaoudi M, et al. Gut Microbes. 2011 Jul-Aug;2(4):256-61.
3) Rao A. V., et al. Gut Pathog. 2009;1:6.